细胞公共制备平台
1、细胞培养工艺发展历程

生物反应器片状载体细胞培养工艺己获国家批准的生物制品(疫苗)
2008年 人用狂犬病疫苗
2016年 EV71型手足口疫苗
2017年 脊髓灰质炎灭活疫苗
2020年 新型冠状病毒肺炎灭活疫苗
2023年 细胞基质流感疫苗
2、一站式智能规模化制备工作站

参照《GMP附录-细胞治疗产品》以及《细胞治疗产品生产现场检查指南》,秉承GMP管理理念,打造规范的细胞治疗产品全流程管理体系。
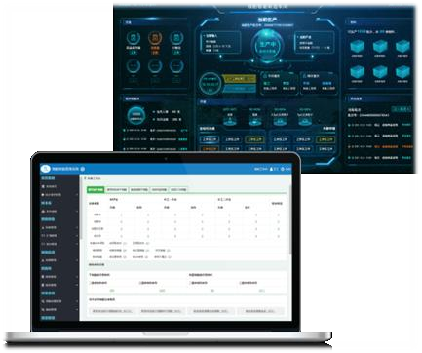
操作简便,手机、平板、电脑,三端无缝交互。已用、高效、便捷、防错。全程一码追溯,扫码即用;系统基于 B/S 架构设计,兼容性强,简单易用;手机 APP、平板 APP、电脑三端互通。
该工作站是一种通用性比较强的移动净化系统,对安装环境没有特殊要求,配备了远程环境检测报警及设备控制系统,为细胞生产提供所需洁净操作环境。
3、智能规模化制备工作站功能
完整实现可配置的多端(医院、运输、机构/工厂)闭环流程:
样本采集-样本运输-细胞制备-细胞质检-细胞存储-细胞应用。模块 、之间信息衔接,通过一物一码设计,建立可视化的样本追踪和细胞溯源体系。
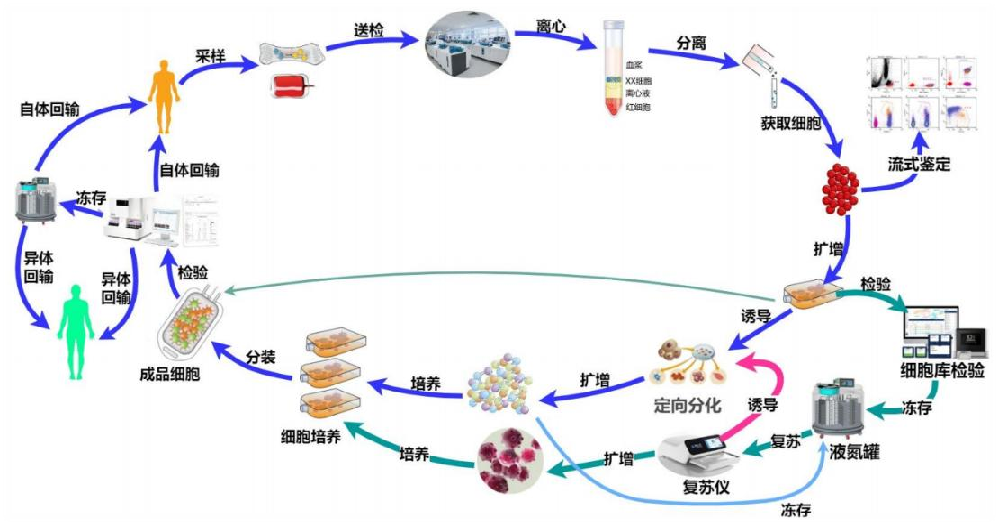

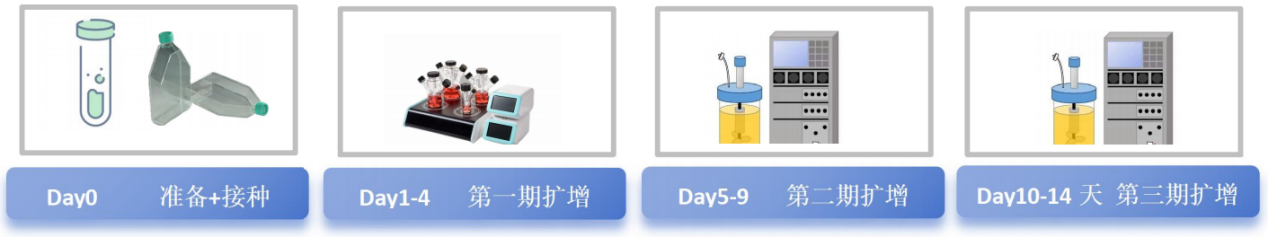
4、规模化细胞培养工艺流程
01高标准工艺设计
采用目前国家批准最先进的生物制品(疫苗)生物反应器细胞培养工艺技术,且为自主研发并获得国家专利认证;细胞培养的片状载体符合生物制品生产要求,主要原辅材料采用药用级或具有药监局药用资质。
02高仿生灌流培养
生物反应器多参数在线实时监控,动态仿生灌流式培养,模拟人体组织细胞生存内环境,并随时智能精准调控温度、PH、溶氧等培养参数,确保细胞一直处于最佳生长环境,从而实现了高质量的规模化细胞培养。
03行业技术性突破
以间充质干细胞培养为例,15L培养体系单批次可收获200亿以上细胞。目前已解决片状载体在细胞培养大规模生产中出现的消化不彻底、回收率低等问题。培养出的细胞尺寸、分泌因子、细胞分化能力等更具优势,且可以增强MSCs的生物学活性。
04满足监管严要求
满足《人源干细胞产品药学研究与评价技术指导原则》的:“尽量采用连续、密闭式生产工艺,减少生产过程中的环境暴露环节,避免污染风险。”以及“部分原材料处在不断更新优化过程中,优先选择风险等级低,如采用药用级的原材料,明确原材料来源、组成、用途”的要求,这些是监管部门倡导的,也是未来细胞培养的大势所趋。
05一站式智能应用
公司自主研发的智能细胞工作站实现了细胞的储存管理、细胞复苏、细胞在线检测及制剂装袋等流程。满足《细胞治疗产品生产质量管理指南》中“宜采用密闭系统或设备进行细胞产品的生产操作”的要求。
06降本增效产业化
该生物反应器片状载体细胞培养工艺技术在实现大规模商业化生产时,较传统人工细胞培养可节省约 90%生产空间、90%人力成本、70%试剂耗材及60%时间成本。
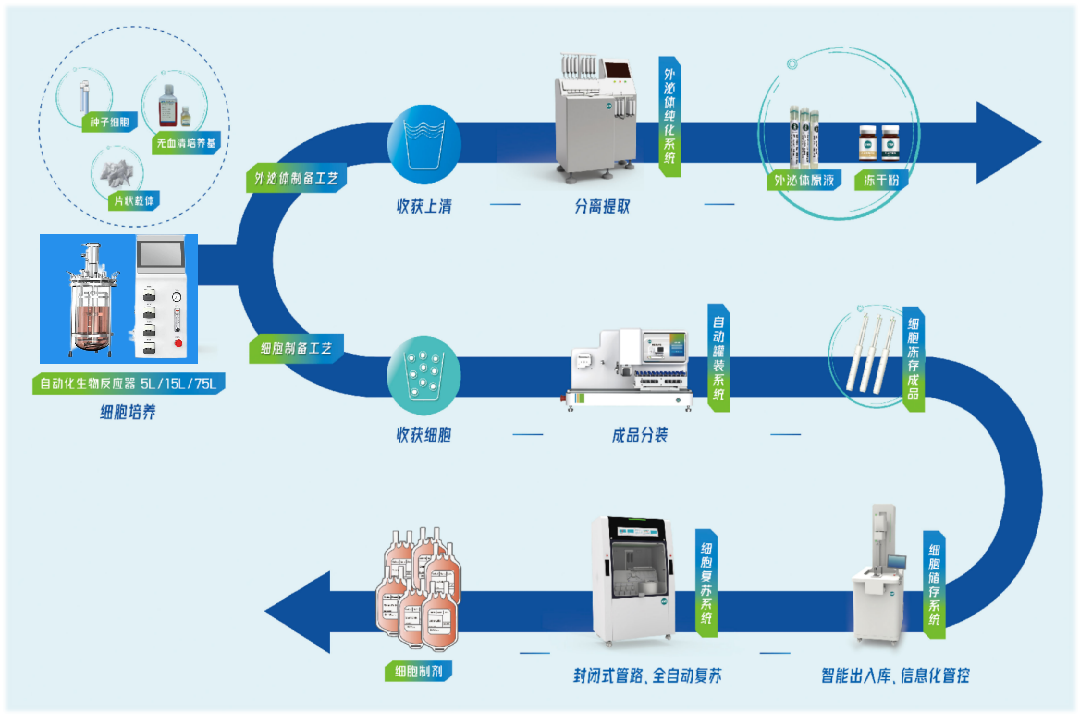
5、生物制品高标准工艺
突破细胞产业化发展瓶颈
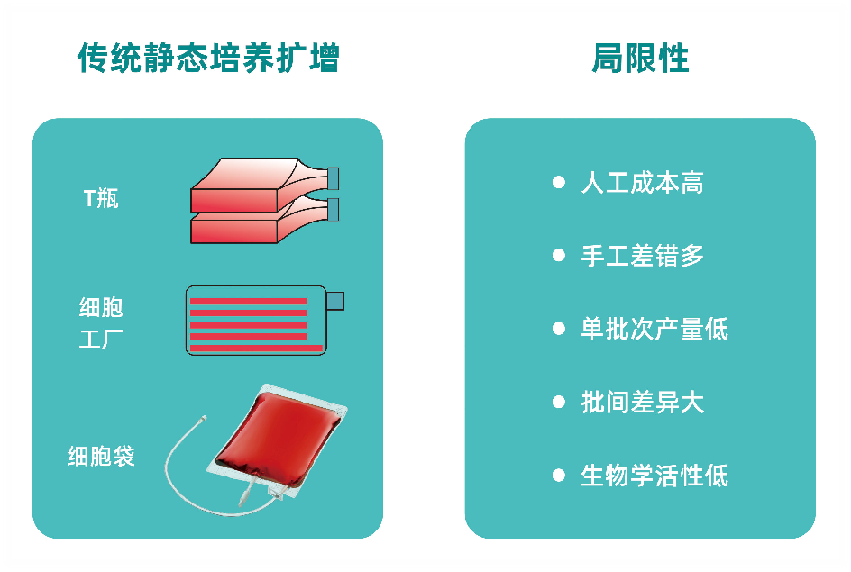
针对细胞培养传统静态扩增工艺中存在人工成本高、手工差错多、单批次产量低、批间差异大、生物学活性低等局限性,重点解决制约细胞治疗产品产业化发展中质不达标、量不充足的瓶颈问题,细胞大规模培养制备工艺是目前的最优解。
工艺采用目前国家批准最先进、最高标准的生物制品(疫苗)生物反应器细胞培养工艺技术,且为自主研发并获得国家专利认证。

6、高仿生灌流培养
生物反应器多参数在线实时监控,动态仿生灌流式培养,模拟人体组织细胞生存内环境,并随时智能精准调控温度、PH、溶氧等培养参数,确保细胞一直处于最佳生长环境,从而实现了高质量的规模化细胞培养。
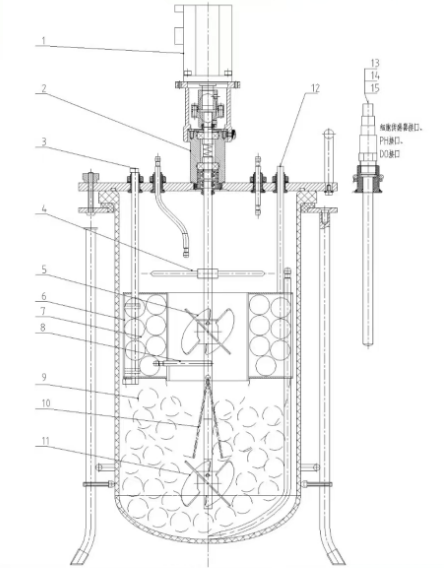
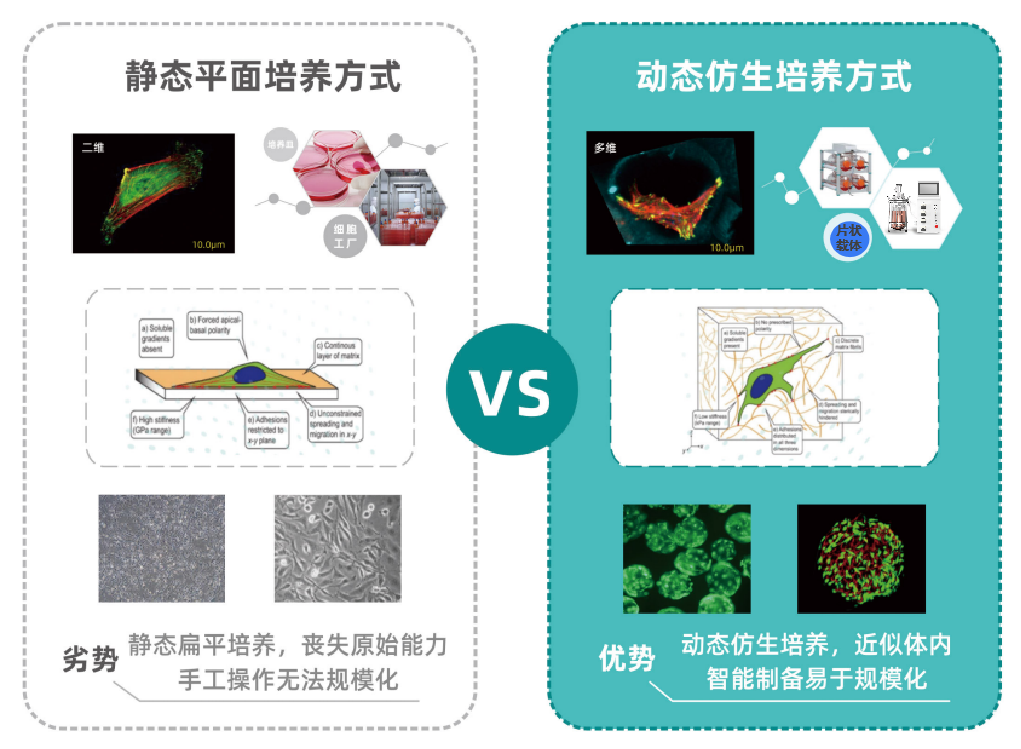
7、行业技术性突破
该工艺较传统人工细胞培养可节省约90%空间、90%人力、60%试剂耗材及60%时间成本。以间充质干细胞培养为例,15L培养体系单批次可收获200亿以上细胞。目前已解决片状载体在细胞培养大规模生产中出现的消化不彻底、回收率低等问题。培养出的细胞尺寸、分泌因子、细胞分化能力等更具优势,且可以增强MSCs的生物学活性。

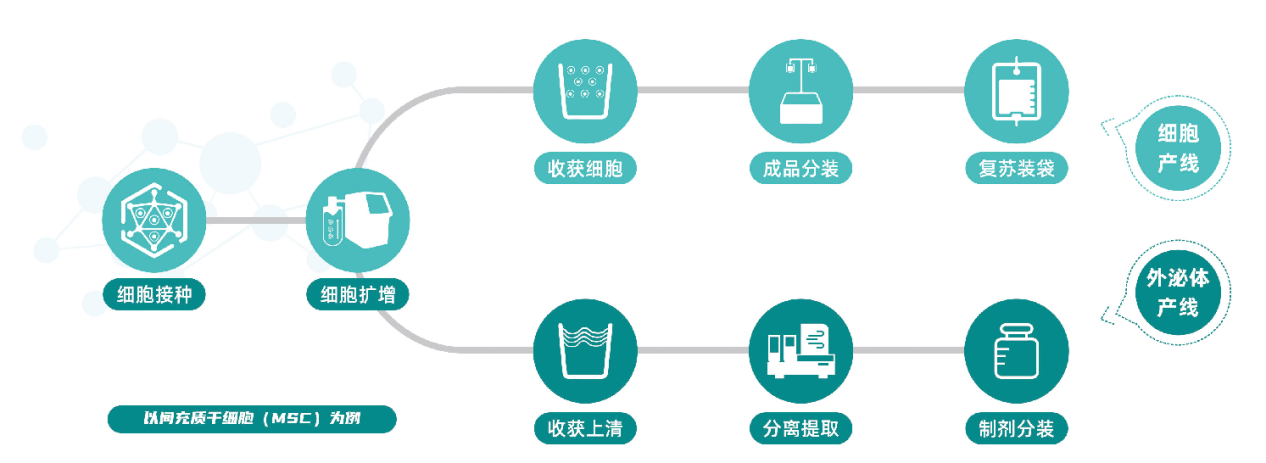
8、一站式智能应用
公司自主研发的智能细胞工作站实现了细胞的储存管理、细胞复苏、细胞在线检测及制剂装袋等流程。满足《细胞治疗产品生产质量管理指南》中“宜采用密闭系统或设备进行细胞产品的生产操作”的要求。


9、检测项目及资质